Koordination:
H. Hausmaninger, Salzburg
Unter Mitarbeit von:
R. Jakesz, Wien
H. D. Kogelnik, Salzburg
H. R. Rosen, Wien
W. Scheithauer, Wien
R. Schiessel, Wien
J. Schüller, Wien
Ch. Sebesta, Wien
F. Sedlmayer, Salzburg
G. Steger, Wien
Problemstellung
Die 5-Jahres-Überlebensraten nach Operation kolorektaler Karzinome sind abhängig von vorgegebenen prognostischen Faktoren und schwanken zwischen 50 und 70% (im Stadium II) bzw. 20-50% (im Stadium III). Von großer klinischer Bedeutung ist das Risiko von Lokalrezidiven nach operiertem Rektumkarzinom. Patienten, bei denen sich syn- oder metachron Metastasen entwickelt haben, haben eine mittlere Lebenserwartung von 10-12 Monaten.
Ziele
Durch eine adjuvante FU/LEV-Therapie kann bei Patienten mit Kolonkarzinom im Stadium III die Rezidivrate um ca. 40% bzw. die Mortalität um 33% gesenkt werden. Patienten mit Rektumkarzinomen (im Stadium II+III) sollten postoperativ kombiniert chemo- und radiotherapeutisch behandelt werden. Bei bereits dissiminierter Erkrankung können in 20-40% der Fälle durch Chemo- (Immun-)therapie Remissionen erzielt werden. Durch eher frühzeitigen Therapiebeginn können sowohl die Lebensqualität als auch das Gesamtüberleben der Patienten günstig beeinflußt werden.
Adjuvante Therapie – Kolonkarzinom
Die 5-Jahresüberlebensraten nach operiertem Kolonkarzinom sind vor allem abhängig vom Tumorstadium, daneben gibt es aber in letzter Zeit auch andere Hinweise, die als „Prognosemarker“ angesehen werden können, wie z.B. Differenzierungsgrad bzw. Ploidy, Zahl der befallenen Lymphknoten und neuerdings auch zytogenetische Faktoren (z.B. Verlust eines Allels auf Chromosom 18q). Während im Stadium II (T3-4N0, Dukes B) der UICC-Klassifikation noch mit einer Heilungsrate von 50-70% nach alleiniger chirurgischer Therapie gerechnet werden kann, sinkt diese bei bereits vorliegendem Lymphknotenbefall (Stadium III bzw. TXN1-3, Dukes C) auf 20-50%. Es wird angenommen, daß bei mehr als der Hälfte der Patienten zum Zeitpunkt der Operation bereits eine (okkulte) Mikrometastasierung vorliegt, weshalb seit mehr als drei Jahrzehnten – vor allem im Rahmen kontrollierter randomisierter Studien – versucht wird, durch systemische Therapie (Chemo- oder Immuntherapie) eine Prognoseverbesserung herbeizuführen.
Als Standardsubstanz in adjuvanten Therapieansätzen gilt der Pyrimidinantagonist 5-Fluorouracil (5-FU). Allerdings konnte mit einer 5-FU-Monotherapie – ebenso wie in der Kombination mit Nitrosoharnstoffen kein signifikanter Übelebensgewinn gegenüber unbehandelten Kontrollgruppen erzielt werden. Lediglich die NSABP (National Surgical Adjuvant Breast and Bowel Project) berichtete über eine signifikante Verbesserung des 5-Jahresüberlebens bei Kolonkarzinomen Dukes B und C durch eine Kombinationsbehandlung mit Methyl-CCNU, Oncovin und 5-FU (MOF).
1989 publizierte eine Arbeitsgrupe aus der Mayo-Klinik die Ergebnisse einer randomisierten Studie, die das Anthelminthikum Levamisol (Lev) allein bzw. in der Kombination mit 5-FU einer Kontrollgruppe gegenüber stellte. Es zeigte sich ein Benefit in der mit 5-FU/Lev behandelten Gruppe, signifikant allerdings nur bei Patienten im Stadium Dukes C. Bei einer von Moertel im Rahmen der Intergroup durchgeführten confirmatory study (die fast 1.300 Patienten inkludierte), wurden die Ergebnisse voll bestätigt. Es zeigte sich bei Patienten im Stadium Dukes C eine Reduktion der Rezidivrate um 41% bzw. der Mortalität um 33% durch eine einjährige Nachbehandlung mit FU/Lev. Daraufhin erklärte ein Expertengremium 1990 bei einer Consensuskonferenz des NIH in Bethesda die Kombination 5-FU/Lev zur Standardtherapie bei Patienten im Stadium III für Patienten außerhalb klinischer Studien. Bei Patienten im Stadium II schienen die Ergebnisse für eine allgemeine therapeutische Empfehlung als nicht ausreichend.
Mittlerweise liegen bereits Ergebnisse mehrerer randomisierter Studien über die Effektivität der Kombination 5-FU und Leucovorin (LV) in der adjuvanten Therapie kolorektaler Karzinome vor. Die Reduktion des Rezidivrisikos beträgt je nach Studie zwischen 35 und 44% bzw. des Mortalitätsrisikos zwischen 22 und 39%. Allerdings wurden dabei unterschiedliche Therapieschemata (5-tägige versus wöchentliche Therapie) verwendet, auch die Dosierung und Behandlungsdauer war different (6 bzw. 12 Zyklen) und es handelt sich durchwegs um 3-Jahresergebnisse).
Eine andere Möglichkeit, die Wirksamkeit von 5-FU durch Biomodulation zu verstärken, ist der kombinierte Einsatz von 5-FU und Interferon-a (IFN-a). Ausgehend von Phase-II-Studien bei metastasierenden kolorektalen Karzinomen, in denen Remissionsraten zwischen 30 und 50% berichtet wurden, wird im Rahmen eines gesamtösterreichischen Protokolls innerhalb der Kooperativen Studiengruppe Mamma und Kolorektale Karzinome eine 5-FU-Monotherapie einer 5-FU/Lev bzw. 5-FU/IFN-a-Therapie bzw. der Kombination 5-FU/Lev/IFN-a gegenübergestellt und untersucht (siehe Abb. 1).
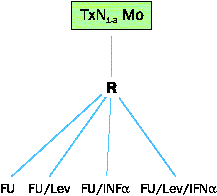
Da im Stadium II bisher kein signifikanter Überlebensgewinn durch adjuvante Chemotherapie publiziert wurde, wird im Rahmen der österreichischen Multicenterstudie (siehe Abb. 2) im Stad. II bzw. T3-4N0 eine unbehandelte Kontrollgruppe mit einem zweiten Arm verglichen, in dem 5-FU zusammen mit dem biologisch aktiven (linksdrehenden) Anteil des Razemats von Leucovorin verglichen wird.
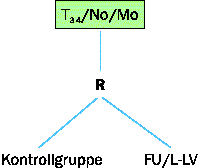
Basierend auf den Überlegungen, daß zum Zeitpunkt der Diagnosestellung kolorektaler Karzinome etwa 20% makroskopisch in die Leber gestreut haben und in Obduktionsstatistiken über 50% der Patienten, die nach kurativer Resektion verstorben waren, metachrone Lebermetastasen hatten und andererseits die Hypothese vertreten wird, daß die Metastasierung vorwiegend über das venöse Drainagesystem erfolgt, wurde bereits vor 20 Jahren mit einer adjuvanten intraportalen Chemotherapie begonnen (erster Bericht Taylor 1979). Obwohl die zu diesem Thema vorliegenden randomisierten Studien verschiedener Arbeitsgruppen untereinander schwer vergleichbar sind und zum Teil über beträchtliche postoperative Komplikationen berichtet wurde, dürfte der therapeutische Benefit etwas geringer sein als mit systemischer adjuvanter Chemotherapie. In einer kürzlich publizierten Metaanalyse von 9 randomisierten Studien betrug die Reduktion des Rezidivrisikos 14% bzw. des Mortalitätsrisikos 13% nach fünf Jahren. Es werden deshalb mit Spannung die Resultate der laufenden randomisierten Studie der SAKK (Schweizer Arbeitsgemeinschaft für Klinische Krebsforschung) – adjuvante intraportale versus systemische Chemotherapie – erwartet. Adjuvante Intraportale Verfahren konnten sich bisher auf breiter Basis nicht durchsetzen.
Seit vielen Jahren werden schließlich auch die Möglichkeiten einer immunmodulierenden Einflußnahme wissenschaftlich untersucht. Eine aktiv-unspezifische Therapie mit BCG führte zu widersprüchlichen Resultaten nach operiertem kolorektalem Karzinom, eine Immunisierung mit autologen oder inaktivierten allogenen Tumorzellen zeigte vielversprechende präliminäre Vorteile gegenüber Kontrollgruppen. Ermutigende Ergebnisse berichtete jedoch eine deutsche Arbeitsgruppe unter Riethmüller. Durch den adjuvanten Einsatz des murinen monoklonalen Antikörpers Mab 17-1 A konnte bei Patienten mit kolorektalem Karzinom eine Senkung der Rezidivrate um 27% und der Mortalität um 30% erreicht werden. Trotz einer 5-jährigen medianen Beobachtungsdauer und der signifikanten Ergebnisse muß diese Studie in einigen Punkten kritisch bewertet werden, vor allem was die Fallzahl von 166 auswertbaren Patienten betrifft. Eine adjuvante Therapie mit monoklonalen Antikörpern erscheint daher vorerst weiterhin nur in klinischen Studien gerechtfertigt.
Diese Ausführungen deuten an, daß sich die therapeutischen Möglichkeiten nach kurativer operativer Therapie von Kolonkarzinomen wesentlich verbessert haben. Während es in den USA seit der Konsensuskonferenz 1990 nicht mehr akzeptiert wird, Patienten mit Dukes C Kolonkarzinomen in einer unbehandelten Kontrollgruppe zu führen, bleibt die überwiegende Mehrzahl der in Österreich operierten Patienten ohne adäquate Nachbehandlung und weniger als 10% aller in Frage kommenden Patienten wurden bisher in die laufende österreichische Adjuvansstudie eingebracht.
Zusammenfassung:
Adjuvante Therapie – Kolonkarzinom: Die therapeutischen Möglichkeiten nach kurativ operierten Kolonkarzinomen konnten in den letzten Jahren entscheidend verbessert werden. Seit ca. fünf Jahren gilt eine Nachbehandlung mit 5-Fluorouracil (5-FU) und Levamisol bei Patienten im Stadium Dukes C als Standardtherapie außerhalb klinischer Studien. Weitere therapeutische Optionen, deren Stellenwert noch nicht ausreichend belegt ist, sind die Kombination 5-FU/Leucovorin, 5-FU/Interferon-a und eine Behandlung mit monoklonalen Antikörpern. Patienten im Stadium Dukes B sollten vorerst nur innerhalb klinischer Studien behandelt werden.
Adjuvante Therapie – Rektumkarzinom
Während im Stadium II (T3-4 N0) noch mit einem 5-Jahresüberleben von etwa 60% gerechnet werden kann, sinkt dieses im Stadium III (TXN1-3) auf ca. 25-30%. Im Gegensatz zum Kolonkarzinom ist neben dem Gesamtüberleben auch die Häufigkeit von Lokalrezidiven von großer klinischer Bedeutung, da diese entscheidende Auswirkungen auf die Lebensqualität der betroffenen Patienten haben können. Das Risiko eines Lokalrezidivs ist stadienabhängig und wird mit 5-10% (im Stadium I) bis 30-50% (Stadium III) angegeben. Daher wurden in klinischen Studien neben systemischen Adjuvansmaßnahmen (Chemotherapie) auch lokaltherapeutische Optionen (Radiotherapie) geprüft. Es besteht Konsens darüber, daß durch Chemotherapie v. a. das Gesamtüberleben beeinflußt wird, während durch eine radiotherapeutische Nachbehandlung lediglich die Lokalrezidivrate signifikant reduziert werden kann, jedoch keine Auswirkungen auf das Überleben nachgewiesen werden konnten.
Medikamentöse Therapie
Analog der Entwicklung der Adjuvanstherapie beim Kolonkarzinom wurden seit Jahren auf 5-FU basierende Behandlungsschemata auch beim operierten Rektumkarzinom geprüft. Während erste positive Auswirkungen auf das Gesamtüberleben mit der Kombination MOF (Methyl-CCNU, Oncovin, 5-FU) innerhalb der NSABP berichtet wurden, zeigte sich in späteren Untersuchungen, daß auf das Nitrosoharnstoffpräparat (Methyl-CCNU) verzichtet werden kann. Schließlich ergab eine Gegenüberstellung von MOF und 5-FU/LV in einer randomisierten Studie (der NSABP) eine klare Überlegenheit der durch Leukovorin modulierten 5-FU-Therapie.
Obwohl spekuliert werden kann, daß die Kombination 5-FU/Lev auch beim Rektumkarzinom gleich wirksam ist wie beim operierten Kolonkarzinom, so liegen diesbezüglich leider keine ausreichenden Daten vor. Das gilt auch für eine Immuntherapie mit monoklonalen Antikörpern (Mab 17-1A), die im Rahmen einer randomisierten deutschen Studie vorwiegend bei Kolonkarzinomen und nur bei einer Minorität von Rektumkarzinomen zum Einsatz kamen.
Da die medikamentöse „Therapie der Wahl“ für sich alleine und vor allem in Kombination mit einer Strahlentherapie derzeit nicht bekannt ist, sollten möglichst viele Patienten innerhalb multizentrischer prospektiv randomisierter Protokolle behandelt werden.
Strahlentherapie
Der optimale Zeitpunkt des Einsatzes einer postoperativen Radiotherapie (RT) wird derzeit kontroversiell diskutiert. Die postoperative RT bietet den Vorteil eines prätherapeutischen exakten Stagings und damit einer besseren Patientenselektion, hingegen den möglichen Nachteil einer schlechteren Vaskularisation und damit narbig bedingten Gewebshypoxie. Hingegen wird durch eine präoperative RT eine bessere Tumordemarkierung und Sterilisierung von Mikrometastasen bei erhaltener Gefäßversorgung diskutiert. Als nachteilig wird die mögliche Übertherapie bei Patienten in günstigeren Tumorstadien empfunden. Obwohl in einer prospektiv randomisierten schwedischen Studie gewisse Vorteile einer präoperativen gegenüber einer postoperativen „Standardbestrahlung“ erkennbar waren, ist aus den publizierten Studien ein direkter Vergleich prä-versus-postoperative Radiotherapie problematisch (unterschiedliche Patientenselektion, unterschiedliche Dosierungen und Methoden), sodaß der günstigste Zeitpunkt für lokale radiotherapeutische Maßnahmen noch zu definieren ist.
Indiziert erscheint aus heutiger Sicht eine adjuvante RT im Stadium Dukes B2 und C, nach Tumorperforation und bei schmalem aboralem Sicherheitsabstand. Zur Anwendung kommt eine isozentrische Drei- oder Vierfeldertechnik in Bauchlage (bei voller Harnblase) im Rahmen von Beschleunigeranlagen. Bestrahlt wird fünf mal wöchentlich in Einzeldosen von 1,8-2 Gy bzw. einer Gesamtdosis von 50 Gy. Eine Brachytherapie ist auf selektierte Situationen beschränkt, eine intraoperative Radiotherapie (IORT) wird an manchen Zentren zusätzlich zu einer prä- und postoperativen perkutanen RT durchgeführt bzw. geprüft.
Kombinierte Radio-und Chemotherapie
In der Absicht, die positiven Auswirkungen einer lokalen RT auf die Frequenz von Lokalrezidiven als auch die Effizienz einer systemischen Chemotherapie hinsichtlich der Verbesserung des Gesamtüberlebens wirksam zu kombinieren, wurden mehrere randomisierte Studien, vor allem von Seiten der GITSG (Gastrointestinal Tumor Study Group) und der NCCTG (North Central Cancer Treatment Group) durchgeführt. Dabei zeigte sich die Überlegenheit eines „combined modality“-Konzeptes. Die Ergebnisse bildeten schließlich auch die Grundlage für die Empfehlungen der NIH-Consensuskonferenz 1990 in Bethesda.
Demnach sollte allen Patienten im Stadium II und III als Standardtherapie eine kombinierte 5-FU und postoperative RT (45-55 Gy) angeboten werden. Es wurde von diesem Expertengremium aber auch darauf hingewiesen, daß zur Optimierung der (multimodalen) Behandlungskonzepte die Durchführung weiterer prospektiv randomisierter Studien dringend erforderlich sei. Diesbezüglich ist auch von Seiten der kooperativen Studiengruppe Mamma- und Kolorektales Karzinom für Patienten mit Rektumkarzinom im Stadium II und III ein weiteres nationales Protokoll geplant.
Für Patienten, die außerhalb eines Protokolls behandelt werden sollen, wird die Beibehaltung der NIH-Empfehlungen vom März 1991 vorgeschlagen:
- Behandlungsbeginn 4-8 Wochen nach Operation
- Chemotherapie in der Woche 1 und 5: 5-FU 500 mg/m2 als Bolus über 5 Tage
- Radiotherapie ab der Woche 9: 45 Gy über 4-6 Wochen, gefolgt von 5,4 Gy Boost in 3 Fraktionen auf das Tumorbett, in Kombination mit 5-FU 500 mg/m2 über 3 Tage in der ersten und letzten Bestrahlungswoche.
- Chemotherapie: 5-FU 450 mg/m2 als Bolus über 5 Tage 4 und 8 Wochen nach Bestrahlung.
Zusammenfassung
Adjuvante Therapie – Rektumkarzinom: Seit einer Empfehlung des NIH-Consensusmeetings 1990 in Bethesda gilt eine kombinierte (5-FU-) Chemo- und Radiotherapie bei Patienten mit operierten Rektumkarzinomen im Stadium II und III als Standardtherapie. Offene Fragen betreffen die optimale Sequenz, Dosierung und Behandlungsdauer der Chemo- und Strahlentherapie. Möglicherweise kann durch neuere medikamentöse Konzepte (5-FU/Lev, 5-FU/LV, monoklonale Antikörper oder andere Immunmodulatoren) eine weitere Verbesserung der Behandlungsresultate nach Rektumkarzinom erzielt werden.
Palliative Therapie des metastasierenden kolorektalen Karzinoms
Bereits zum Zeitpunkt der Diagnose eines kolorektalen Karzinoms liegen bereits bei 20-25% der Patienten synchrone Absiedelungen vor, bei etwa der Hälfte aller operierten Patienten entwickeln sich im weiteren Verlauf metachron Rezidive bzw. Metastasen, die zu 80% intraabdominell gelegen sind, bzw. in etwa der Hälfte der Fälle die Leber betreffen und es stellt sich die Frage einer pallliativen medikamentösen Therapie.
Trotz umfassender klinischer Prüfung aller heute verfügbaren Zytostatika und Immuntherapeutika gilt der Antimetabolit 5-FU seit über drei Jahrzehnten als wirksamste Einzelsubstanz bzw. als Standardtherapie. Die Rate an objektiven Tumorrückbildungen liegt allerdings in neueren randomisierten Studien nur bei ca. 10%, die Remissionen sind fast ausnahmslos partiell und auf nur wenige Monate beschränkt. Ein Einfluß auf die Überlebenszeit gilt als nicht gesichert.
Neuere Strategien beinhalten die Erhöhung der therapeutischen Effizienz von 5-FU durch biochemische Modulatoren, die Entwicklung neuerer Substanzen und der selektive Einsatz einer regionalen Chemotherapie bei isoliertem Leberbefall. Obwohl das optimale Regime noch nicht definiert ist, konnte durch die Kombination von 5-FU/Leucovorin (LV) und die Auswertung der Behandlungsergebnisse innerhalb einer Metaanalyse von neun randomisierten Studien eine Remissionsrate von 23% (gegenüber 11% durch 5-FU-Monotherapie) nachgewiesen werden, der Einfluß auf das Gesamtüberleben war jedoch nur marginal unterschiedlich. Ähnliche Verbesserungen wurden auch mit der sequentiellen Verabfolgung von Methotrexate und 5-FU erarbeitet. In der Metaanalyse 8 randomisierter Studien zeigte sich eine Remissionsrate von 19% (versus 10% durch FU-Monotherapie). Als weitere Möglichkeit der Modulation der 5-FU-Wirkung bot sich Interferon-a (IFN-a) an, nach dem an humanen Kolonkarzinomzellinien ein Synergismus zwischen 5-FU und IFN-a nachgewiesen wurde. In verschiedenen Phase-II-Studien wurden mit dieser Kombination vorerst Ansprechraten von 70% berichtet, in der Folge allerdings auf 20-40% relativiert. In einer großen gesamtösterreichischen Palliativstudie wurde durch die Doppelmodulation von 5-FU mit LV und Interferon ein objektives Tumoransprechen in fast 40% der Fälle erzielt, allerdings im Vergleich mit der “Standardtherapie” 5-FU/LV kein Überlebensgewinn beobachtet.
An neueren Substanzen stehen heute neue Platinanaloga, Taxane, Gemcitabine und vor allem Camtothecin-11, das erste interessante Ergebnisse bei vorbehandelten Patienten erkennen ließ, zur Verfügung. Es müssen jedoch weitere Untersuchungen abgewartet werden, bevor der Stellenwert dieser Medikamente beurteilt werden kann.Zur Frage des Behandlungsbeginnes – vor allem bei asymptomatischen Patienten – kann das Ergebnis zumindest zweier randomisierter Studien herangezogen werden, die nachgewiesen haben, daß durch sofortigen Einsatz der Chemotherapie (zum Zeitpunkt der nachgewiesenen Metastasierung) sowohl eine längere Symptomfreiheit bzw. bessere Lebensqualität als auch ein Überlebensbenefit ermöglicht wird.
Regionale Chemotherapie
Während normales Leberparenchym vorwiegend über die V. portae versorgt wird, erfolgt die Blutversorgung von Lebermetastasen vor allem über die A. hepatica. Es wurden daher bereits seit den 50er Jahren intraarterielle (i.a.) Chemotherapien durchgeführt, aber erst in letzter Zeit wurde durch die Entwicklung von implantierbaren Kathetern (Port-a-Cath) und auch implantierbare (Infusaid 400) oder tragbare externe (Pharmacia Deltec) Pumpensysteme eine Anwendung auf breiterer Basis ermöglicht. Der Vorteil der i.a. Chemotherapie ist eine selektivere Erreichbarkeit neoplastischen Gewebes gegenüber normalem Lebergewebe und eine höhere hepatale Wirkstoffkonzentration gegenüber der systemischen Anwendung bei gleichzeitig limitierter systemischer Toxizität. In verschiedenen Phase-II-Studien wurden vor allem 5-FU und Flourodesoxyuridin (FUDR), aber auch BCNU, Mitomycin C, Cisplatin und Adriamycin i.a. appliziert und bei einem medianen Überleben von 17 Monaten Remissionsraten von im Mittel 50% mitgeteilt (Ergebnisse von 9 Studien an 375 Patienten). Auch innerhalb von sieben randomisierten Studien zeigten sich durchwegs signifikante Tumorrückbildungsraten (40-60%) einer i.a. gegenüber einer systemischen (intravenösen) Chemotherapie (Remissionsraten 10-20%). Die Beurteilung (vor allem hinsichtlich eines etwaigen Überlebensgewinnes) wird jedoch dadurch erschwert, daß zum Teil ein Cross over (i.a. Therapie nach Versagen einer systemischen Behandlung) erlaubt war, in manchen Studien im Kontrollarm lediglich eine 5-FU-Monotherapie oder nur eine Supportivbehandlung allein (fakultativ) zum Einsatz kamen und die Fallzahlen zum Teil als nicht ausreichend bezeichnet werden müssen. Erst kürzlich publizierten allerdings englische Autoren (Allen Mersh et al., Lancet 1994) die Ergebnisse einer randomisierten Studie an 100 Patienten, wobei eine i.a. FUDR-Therapie mit rein symptomatischen Maßnahmen verglichen wurde. Es zeigte sich neben einer signifikanten Verlängerung der Überlebenszeit (405 vs. 226 Tage) auch eine Verbesserung der Lebensqualität der i.a. behandelten Patienten. Allerdings dürfen in den Überlegungen hinsichtlich der Indikationsstellung für eine i.a. Chemotherapie die zum Teil beträchtlichen Nebenwirkungen (direkte Hepatotoxizität, biliäre Sklerose, chronische Gastritis bzw. Ulcerationen, Nausea, Vomitus und Diarrhoe) bzw. Katheterprobleme nicht vernachlässigt werden und sind stark abhängig von der Operationstechnik bzw. Erfahrung des implantierenden Chirurgen.
Neuere Intentionen zur Verbesserung der Ergebnisse der regionalen Chemotherapie betreffen die Kombination von Pyrimidinantagonisten mit LV oder IFN-a oder die Kombination von i.a. mit systemischen Chemotherapieprogrammen zur Hintanhaltung einer extrahepatalen Progredienz der Erkrankung.
Daneben stellt die Verbindung einer Zytostatikaapplikation mit (meist temporär) i.a. Gefäßokklusion wie zum Beispiel mit Stärkemikrosphären (Spherex) in Form einer Chemoembolisation eine neuere therapeutische Option dar. Obwohl zum Teil ein besseres Tumoransprechen bei zusätzlicher Embolisation gegenüber konventioneller i.a. Therapie berichtet wurde, sind für eine endgültige Beurteilung dieses Verfahrens weitere (vor allem randomisierte Untersuchungen) notwendig. Als Indikation für ein regionales Therapieverfahren können angesehen werden:
- chirurgisch nicht resezierbare Lebermetastasen
- 4 Lebermetastasen
- isolierter Leberbefall
- adäquate Leberfunktion und Allgemeinzustand
Progression nach systemischer Chemotherapie
Zusammenfassend kann festgestellt werden, daß sich das therapeutische Armamentarium bei Patienten mit fortgeschrittenen kolorektalen Karzinomen wesentlich verbessert hat. Die Indikationsstellung für den Beginn einer Palliativtherapie, die Auswahl des jeweiligen Therapieverfahrens, sowie das erforderliche exakte Monitoring der Patienten hinsichtlich zu erwartender Nebenwirkungen erfordern jedoch ausreichende onkologische Erfahrung des behandelnden Arztes.
Zusammenfassung:
Palliative Therapie des metastasierten kolorektalen Karzinoms: Als Standardsubstanz in der Behandlung fortgeschrittener kolorektaler Karzinome gilt nach wie vor 5-Fluorouracil (5-FU). Da mit einer Monotherapie allerdings nur in etwa 10% der Fälle eine Remission erreicht werden kann, wird heute zumeist eine Modulation der FU-Wirkung mit Leucovorin oder Interferon-a bzw. auch Doppelmodulationen durchgeführt, wordurch sich die Tumorrückbildungsrate auf 20-40% bei allerdings nicht gesichertem Überlebensgewinn anheben ließ. Bei isoliertem Leberbefall stellt eine regionale Chemotherapie eine weitere sinnvolle therapeutische Option dar, die allerdings nur an Zentren mit ausreichender Erfahrung durchgeführt werden sollte.
